作者: Paul A. Webb
本文是题为 “Chemical Adsorption“ 的更全面文章的精简版。
简介
催化剂广泛应用于从消费品生产到环境保护的各种领域。催化剂的优化设计和有效利用需要对活性材料的表面结构和表面化学有全面的了解。化学吸附分析技术提供了催化剂在设计和生产阶段以及使用一段时间后,评估其材料性能所需的大量信息,尤其是本文中要介绍的多相催化剂。
物理吸附和化学吸附的区别
固体材料的一个显著特征是结合气体或蒸汽分子的弱表面能位点分布,也就是能发生气体吸附现象。表面吸收的分子量取决于若干条件和表面特征,比如温度、压力、表面能分布和固体的表面积。恒温下吸附的分子量与压力的关系图称为吸附等温线。
物理吸附是固体表面和吸附质之间相对较弱的范德华作用力(物理吸引力)的结果。物理吸附是可逆现象。
不同吸附质和固体表面之间也可能发生电子共享,形成化学键,发生化学吸附现象。与物理吸附不同,化学吸附是不可逆的,通常需要额外的能量来去除化学吸附的分子。
在合适的温度和压力条件下,所有表面均可发生物理吸附。而化学吸附仅发生在某些吸附剂和吸附质之间,且仅在干净的表面上。
在适当的条件下,物理吸附可以发生多层吸附。另一方面,化学吸附仅在吸附剂能够与表面直接接触的情况下进行,一般是单层吸附。
物理吸附的一个特征是,几乎所有吸附的分子都可以在发生吸附的相同温度下通过真空脱附。加热可为吸附分子提供从吸附位点脱附所需的能量,加速脱附。
化学吸附的分子强烈地结合在表面上。相比物理吸附分子的脱附,如果没有相对大量的能量流入,化学吸附的分子不容易从位点上脱附。因此,通常需要非常高的温度从表面上脱附化学吸附的分子。
物理吸附一般在某个压力下接近或低于吸附剂沸点的温度下发生。而化学吸附通常可以在远高于吸附剂沸点的温度下发生。
化学吸附与催化的关系
催化剂能影响化学反应速率而不改变化学平衡,只能改变反应接近平衡的速率,不能够催化本身不会发生的化学反应。“活性” 金属的表面由化学吸附位点组成。负载型催化剂是指活性金属以细颗粒分散在载体上的催化剂。位于载体表面的颗粒可与吸附剂反应。如果加速的反应速率仅仅是由于表面分子浓度的增加,则催化作用可由反应物的物理吸附产生。如果是化学吸附使得反应物(吸附分子)更容易发生化学反应,则催化作用是由形成的活性表面键中间体产生的。这也是化学吸附作为分析技术在催化研究中非常重要的原因之一。
多相催化反应循环的阶段为:
1)反应物向催化剂表面的扩散 (传输)
2)反应物的化学吸附
3)化学吸附物种间的表面反应
4)产物从催化剂表面的脱附
5)产物从催化剂表面扩散
可采用物理吸附和压汞法等分析技术预测步骤 1 和 5 的速率,比如表征催化材料的孔隙率。表征步骤 2、3 和 4 则是化学吸附分析的领域。
催化剂评价的化学吸附技术和方法
化学吸附分析可用于确定催化剂在促进特定反应中的相对效率,或用于研究催化剂中毒和监测催化剂随使用时间的失效行为。
等温化学吸附分析可分为:a) 静态体积化学吸附和 b) 动态(流动气体)化学吸附。静态化学吸附可从接近环境至 1000°C 或更高的任何温度下,从低压到大气压力下得到化学吸附等温线,获得高分辨率测量。
脉冲化学吸附是一种流动气体技术,通常在环境压力下进行。在惰性气体流中预处理样品,注入少量吸附质直到样品饱和。校准好的热导率检测器(TCD)用于测量每次注射时活性位点吸附的吸附质分子量。初始注射可能发生完全吸附。吸附饱和后,再次注射不会发生化学吸附。化学吸附的气体分子数与材料的活性表面积直接相关。
每克样品化学吸附的气体量,结合反应的化学计量数和催化剂制备过程中与载体混合的活性金属量,可以计算金属分散度,这是催化剂性能的重要指标,也是计算催化剂中昂贵活性金属效率的重要经济指标。
脉冲化学吸附
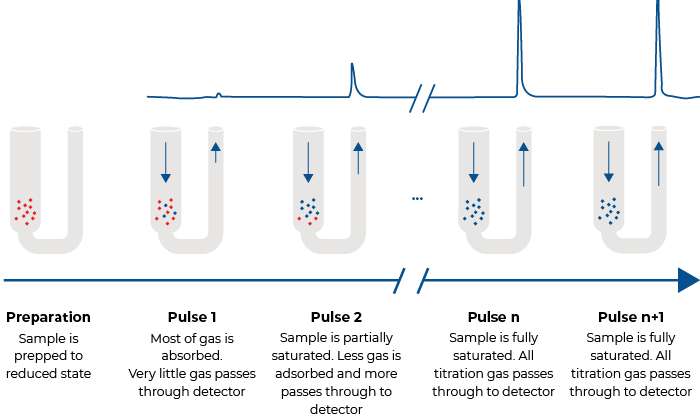
程序升温脱附 (TPD)、程序升温还原 (TPR) 和程序升温氧化 (TPO) 是表征催化剂的三种非等温方法。程序升温脱附通常不采用真空,能够更好地模拟实际工况。在 TPD 分析中,将材料放入样品管进行预处理,得到干净的活性表面。接下来,将选定的气体或蒸汽化学吸附在活性位点上,直到达到饱和,然后用惰性气体吹扫残余气体。
在恒定的惰性流动气体氛围中,以可控速率升高温度。当热能超过结合能时,吸附质从活性位点上脱附出来,由热导检测器检测惰性气体和脱附的分子量。TCD 信号与脱附的分子量成正比。在特定温度下脱附的量提供了关于化学吸附位点的数量、强度和异质性等信息。
程序升温脱附 (TPD)
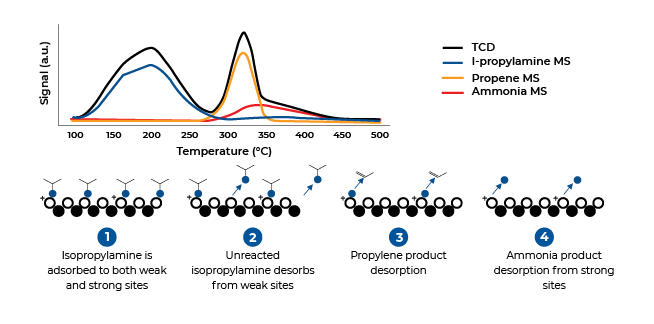
程序升温还原 (TPR)
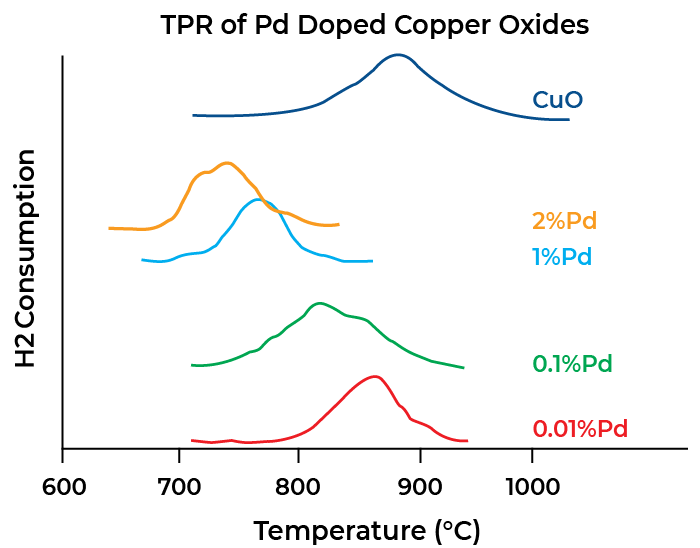
程序升温还原主要用于研究分散在载体上的金属氧化物还原性能。在程序升温过程中,将稀释的氢(或另一种还原气体)通入样品中,测量氢的消耗量和发生还原的温度分布。氢消耗量与温度的关系图有一个或多个峰,获得的数据反应了样品中可还原物种的数量以及它们的活化能。
表面能
当固体表面暴露于吸附质时,能量最高的位点首先被占据。特定表面覆盖度下的吸附热可使用克劳修斯 – 克拉佩龙方程计算。该表达式描述了压力、温度和气体常数之间相互关系的等位吸附热,特别适用于通过静态体积吸附技术获得的数据。
在一定覆盖度范围内的等位吸附热可以从等量吸附线中获得,这是恒定吸附体积下压力与温度的曲线图。从同一材料在不同温度下获得的一系列等温线中提取等量吸附线。在对数标度 (lnP vs 1/T)ₙ上绘制的等量吸附线斜率提供了一个数据点 (qₛₜ, n),其中 n 是与等量吸附线相关的覆盖度。不同覆盖度的等量吸附线描述了表面能与覆盖度的关系,该信息有助于预测催化剂在特定温度下对特定化学反应的活性。
活化能也可以从动态化学吸附技术(特别是 TPD)获得的数据中推导。该方法的过程与静态体积技术的过程相反。加热升高温度,吸附质分子从最弱的位点上开始脱附。脱附的分子被吹扫,不再发生二次吸附。表面覆盖度的变化与温度的变化率有关。
简单分子的脱附速率可以使用一级动力学建模,通常表示为 -kq,其中 k 是速率常数,负号表示覆盖度随时间的减少,q 表示当前的表面覆盖度。
速率常数 k 可用 Arrhenius 形式表示,即 exp (-Eₐ/RT),其中 Eₐ 是脱附的活化能,T 是绝对温度,R 是气体常数。A 是指前因子。
结合上述关系和方程,最终得出可通过 TPD 分析确定变量的活化能表达式。
结论
化学吸附是多相催化的基本过程。了解与催化剂和反应物相关的化学吸附过程是控制催化剂的组成、催化剂制备以及催化剂评价的关键。因此,能够测量化学、物理吸附和脱附等温线的分析仪器以及能够分析程序升温反应的分析仪器是研究催化作用的有力工具。